Bildverarbeitung im Fliegenhirn
Forschungsbericht (importiert) 2014 - Max-Planck-Institut für Neurobiologie
Was wir "sehen", ist errechnet
Wenn wir die Augen öffnen und umherblicken, erkennen wir in Sekundenbruchteilen, wo wir uns befinden, und wissen, welche Gegenstände uns umgeben. Wir erkennen ein Buch, sehen seine Farbe, wir wissen, wie weit entfernt von uns das Buch steht. Alle diese Informationen sind zwar in den Bildern vorhanden, die unser Gehirn von der Netzhaut empfängt, aber nicht explizit: Um diese Informationen zu erhalten, muss unser Gehirn rechnen. Dies wurde in vollem Umfang deutlich, als man das erste Mal versuchte, Computer so zu programmieren, dass sie, mit einer Kamera verbunden, die gleichen Informationen ausgeben, die wir Menschen so leicht aus den Bildern lesen. Wie aber errechnet das Nervensystem die Informationen aus den Bildern, die von den Augen geliefert werden? Diese Frage untersuchen die Wissenschaftler in der Abteilung Schaltkreise – Information – Modelle am MPI für Neurobiologie am Beispiel des Bewegungssehens. Neben dem Erkennen von Gegenständen, der Tiefe im Raum und seiner Farbe ist Bewegung eine der wichtigsten Bildinformationen: Wir benutzen Bewegungsinformation, um unseren Weg zu steuern, wir benutzen sie, um uns schnell auf den Gehsteig zu retten, wenn wir beim Überqueren der Straße ein herannahendes Auto sehen, oder wir benutzen sie, wenn wir einen Ball fangen wollen, der uns zugeworfen wird.
Warum die Fliege?
Die Martinsrieder Forscher untersuchen dieses Problem aus mehreren Gründen am Sehsystem der Fliege: Zum einen ist die Fliege als schnell fliegendes Insekt auf Sehen und dabei speziell auf das Sehen von Bewegungen spezialisiert. Mehr als 50 Prozent aller Nervenzellen im Fliegengehirn sind einzig der Bildverarbeitung gewidmet. Zum anderen besteht das Gehirn der Fliegen aus nur wenigen 100 000 Nervenzellen. Dies ist im Vergleich zu den circa 100 Milliarden Nervenzellen des menschlichen Gehirns eine nahezu bescheidene Anzahl, was die Analyse entscheidend erleichtert. Darüber hinaus steht der Forschung bei der Fruchtfliege Drosophila eine große Menge genetischer Methoden zur Verfügung, um Nervenzellen gezielt zu manipulieren: Dabei legt ein Gen fest, welches Protein in der Zelle erzeugt wird, ein anderer Genabschnitt legt die Adresse fest, also in welcher Zelle dies geschehen soll. Die Möglichkeiten sind schier unerschöpflich: (i) Es gibt Proteine, welche die Nervenzellen blockieren. Ist in Tieren, bei denen zum Beispiel Zelle A blockiert ist, die Reaktion auf Bewegungsreize deutlich gestört, weiß man, das Zelle A am Bewegungssehen beteiligt ist. (ii) Andere Proteine erhöhen ihre Fluoreszenz, wenn die Nervenzelle aktiv ist. Damit lassen sich die Antworten der Nervenzellen auf Bewegungsreize mit dem Mikroskop optisch messen. (iii) Schließlich können auch Proteine in die Zellen eingebracht werden, welche bei Belichtung die Zelle aktivieren. Diese ‚optogenetische‘ Methode erlaubt es, die Verschaltung zwischen einzelnen Nervenzellen nachzuweisen, indem man eine Zelle anregt und die Aktivität in der nachgeschalteten Zelle misst.
Das Sehsystem der Fliege
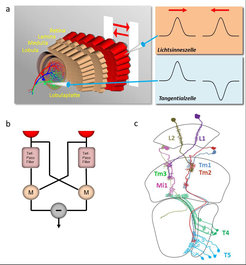
Das Sehsystem der Fliege beginnt mit den großen Facettenaugen. In jeder Facette liegen acht Lichtsinneszellen. Anders als oft angenommen sieht dabei jede einzelne Facette nur einen kleinen Bildpunkt, liefert also zum Gesamtbild im Gehirn nur einen einzelnen Pixel. Der hinter den Augen liegende ‚optische Lobus‘ besteht aus vier Schichten von Nervenzellen, welche sich in einzelne Kolumnen (Säulen) gliedern (Abb. 1a). Diese Kolumnen entsprechen in Anzahl und Anordnung genau den Facetten des Auges und enthalten ungefähr je 100 Nervenzellen. In der Fruchtfliege Drosophila gibt es ca. 750 Facetten pro Auge und entsprechend nur 750 solcher Kolumnen. Das Bild wird also in lediglich 750 Pixeln im Gehirn repräsentiert. Bewegt sich nun ein Objekt von links nach rechts und wieder zurück, antwortet eine einzelne Lichtsinneszelle beide Male gleich (Abb. 1a). Offensichtlich ist die Information über die Bewegungsrichtung also nicht aus den Signalen einer einzelnen Lichtsinneszelle ablesbar. Geht man aber stattdessen zu einer der großen Tangentialzellen, die sich in der 4. Schicht, der sogenannten ‚Lobulaplatte‘ befinden, erhält man ein anderes Bild: Hier reagieren die Zellen auf Bewegung in eine Richtung mit einer elektrischen Erregung, auf Bewegung in die andere Richtung mit einer Hemmung. Die Signale sind richtungsselektiv. Innerhalb weniger Verknüpfungsstellen wird also aus den richtungsunspezifischen Signalen der Lichtsinneszellen ein richtungsselektives Signal errechnet. Wie kann das sein?
Der Hassenstein-Reichardt-Detektor
Schon vor mehr als 50 Jahren schlugen Bernhardt Hassenstein und Werner Reichardt ein Modell vor, welches genau dieses Phänomen erklärt (Abb. 1b). Um die zeitliche Abfolge der Signale in zwei benachbarten Sinneszellen und damit die Bewegungsrichtung zu erkennen, wird das Signal einer Lichtsinneszelle durch einen sog. Tiefpass-Filter zeitlich verzögert und anschließend mit dem nicht-verzögerten Signal der Nachbarzelle multipliziert. Wird diese Operation in zwei zueinander spiegelbildlichen Einheiten durchgeführt und deren Signale anschließend voneinander subtrahiert, erhält man am Ausgang eine richtungsselektive Antwort: Bewegt sich das Objekt von links nach rechts, ist die Antwort positiv, bewegt sich das Objekt von rechts nach links, ist die Antwort negativ, genau wie das elektrische Signal der oben beschriebenen Zelle in der Lobulaplatte der Fruchtfliege.
Das Modell beschreibt den Mechanismus des Bewegungssehens auf einer abstrakten, mathematischen Ebene. Dies ist ein großer Vorteil, weil man mithilfe von Computersimulationen präzise Vorhersagen machen kann, was man in den bewegungsempfindlichen Zellen der Lobulaplatte zu erwarten hat. Tatsächlich wurden auf diese Weise eine Vielzahl von Simulationen und Experimenten gemacht, welche das Modell in allen Punkten bestätigten. Das Modell beschreibt also die Verschaltung zwischen den Facettenaugen und der Lobulaplatte sehr exakt. Es sagt aber überhaupt nichts darüber aus, welche Nervenzellen des optischen Lobus an dieser Verschaltung beteiligt sind. Die entsprechenden Schaltkreise blieben lange Jahre im Dunkeln. Erst in den letzten Jahren gelang es mithilfe der oben beschriebenen genetischen Methoden, die Nervenzellen zu identifizieren, die den verschiedenen Elementen des Hassenstein-Reichardt-Modells entsprechen und die Information über die Bewegungsrichtung aus den Bildern extrahieren (Abb. 1c).
ON- und OFF-Kanäle
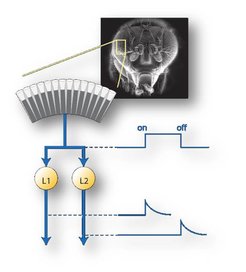
In der ersten Schicht des optischen Lobus, der sogenannten ‚Lamina‘, kontaktieren die Lichtsinneszellen des Facettenauges in jeder Kolumne fünf verschiedene Lamina-Zellen, die wiederum mit unterschiedlichen Nervenzellen in der nächsten Schicht verbunden sind. Offensichtlich wird die primäre Bildinformation also in verschiedene, parallele Kanäle geleitet und dort spezifisch weiter verarbeitet. Welcher dieser Kanäle bildet den Eingang zum Bewegungs-Detektor? Diese Frage konnte durch gezielte Blockierung der verschiedenen Lamina-Zellen beantwortet werden [1]. Wurde die Zelle L1 blockiert, war die Bewegungsantwort auf ca. 50 Prozent reduziert, wurde die Zelle L2 blockiert, ebenfalls. Wurden beide Zellen – L1 und L2 – blockiert, konnte keine Bewegungsantwort mehr beobachtet werden. Daraus konnte geschlossen werden, dass L1 und L2 die Haupteingänge zum Bewegungsdetektor darstellen. Was aber war der Unterschied zwischen den beiden Kanälen? Dies wurde deutlich, als die Wissenschaftler statt regelmäßiger Muster Hell- und Dunkel-Kanten als Bewegungsreize verwendeten: Bei Blockierung von L1 war die Antwort auf Hell-Kanten verschwunden, während die Antwort auf Dunkel-Kanten intakt war. Das umgekehrte wurde bei Blockierung von L2 beobachtet: Hier war die Antwort auf Hell-Kanten intakt, während die Antwort auf Dunkel-Kanten gleich Null war. Diese und weitere Experimente belegten, dass im Fliegengehirn die primäre Information über Helligkeit, je nach ihrer zeitlichen HelligkeitsÄnderung aufgespalten und in zwei parallelen Kanälen analysiert wird (Abb. 2): Die Laminazelle L1 bildet den Eingang zum ON-Kanal, der die Bewegungsrichtung von Hell-Kanten errechnet, die Laminazelle L2 bildet den Eingang zum OFF-Kanal, der die Bewegungsrichtung von Dunkel-Kanten errechnet.
T4- und T5-Zellen
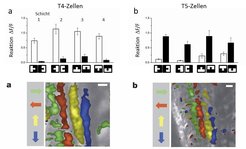
Bereits seit längerer Zeit legten anatomische Befunde zwei Bahnen durch den optischen Lobus nahe: eine L1-Bahn, welche über sogenannte T4-Zellen in die Lobulaplatte geht, und eine L2-Bahn, die über sogenannte T5-Zellen in das gleiche Zielgebiet führt. Daher war es naheliegend, im nächsten Schritt die Signale von T4- und T5-Zellen auf bewegte ON- und OFF-Kanten zu untersuchen. Dies gelang den Wissenschaftlern im vergangenen Jahr [2] und belegte die oben beschriebene Aufspaltung in ON- und OFF-Kanäle eindrucksvoll (Abb. 3 a,b): Während T4-Zellen selektiv auf die Bewegung von ON-Kanten reagieren, sprechen T5-Zellen selektiv auf die Bewegung von OFF-Kanten an. Weiterhin zeigten die Untersuchungen, dass sich beide Zelltypen in je vier funktionelle Untergruppen aufteilen (Abb. 3 a,b): Eine Gruppe von T4/T5-Zellen reagiert maximal auf Bewegung von vorne nach hinten vor dem Fliegenauge und projiziert in die vorderste Schicht 1 der Lobulaplatte. Eine andere Gruppe reagiert maximal auf Bewegung von hinten nach vorne und projiziert in Schicht 2. Eine dritte Gruppe reagiert maximal auf Aufwärtsbewegung und projiziert in Schicht 3, eine vierte Gruppe reagiert maximal auf Abwärtsbewegung und projiziert in Schicht 4. In der Lobulaplatte läuft die Information der ON- und OFF-Kanäle wieder zusammen: T4- und T5-Zellen kontaktieren gemeinsam in der entsprechenden Schicht die großen Tangentialzellen. Bei Blockierung von T4- oder T5-Zellen reagieren die Tangentialzellen spezifisch auf Hell- bzw. Dunkel-Kanten nicht mehr, genau so, als hätte man die Laminazellen L1 oder L2 blockiert.
Diese Befunde sind in vielfacher Hinsicht erstaunlich. Zum einen gleicht der Aufbau des Bewegungs-Sehsystems bei der Fliege in mehreren Punkten der Informationsverarbeitung in der Netzhaut der Wirbeltiere: Auch dort werden die Signale der Lichtsinneszellen zunächst in parallele ON- und OFF-Kanäle aufgespalten und Bewegungsinformation in beiden Bahnen separat berechnet. Im nächsten Schritt wird diese Information von ON- und OFF-Kanälen auf der Ebene von richtungsspezifischen Ganglion-Zellen zusammengebracht. Wie bei der Fliege existieren davon vier Untergruppen für die vier orthogonalen Hauptrichtungen. Dies ist umso erstaunlicher, als bei der Fliege die visuelle Umwelt zunächst in einem hexagonalen Raster vorliegt. Dennoch wird an einer Stelle der Informationsverarbeitung von dem hexagonalen in ein orthogonales Koordinatensystem umgerechnet. Für all die genannten Gemeinsamkeiten scheint in der Evolution ein großer Selektionsdruck am Werke gewesen zu sein.
Zusammenfassung und Ausblick
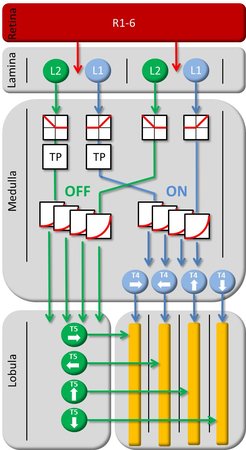
Die Erforschung des Bewegungssehens bei der Fliege hat dank des Einsatzes genetischer Methoden erstaunliche Fortschritte gemacht. Heute ist bekannt, dass die Bewegungsrichtung in separaten ON- und OFF-Kanälen errechnet wird und durch die T4- und T5-Zellen, sortiert nach den vier orthogonalen Hauptrichtungen, in der Lobulaplatte vorliegt (Abb. 4). Eine naheliegende Frage ist, ob T4- und T5-Zellen die einzigen bewegungsempfindlichen Zellen im Fliegengehirn sind. Oder gibt es dazu parallel noch andere Verarbeitungsbahnen, die auf visuelle Bewegung reagieren? Die klare Antwort lautet: Nein. Werden beide Gruppen von Neuronen blockiert, sind die Fliegen absolut bewegungsblind. Sie reagieren weder auf die Bewegungsrichtung großflächiger Muster, noch auf die Bewegungsrichtung kleiner Objekte.
Eine große Wissenslücke existiert aber immer noch: Was passiert zwischen den Lamina-Zellen L1 und L2 und den bewegungsempfindlichen T4- und T5-Zellen? Jüngste Untersuchungen haben eine Reihe von Neuronen identifiziert, welche die L1-Zellen mit den T4-Zellen verbinden, ebenso diejenigen, welche die L2-Zellen mit den T5-Zellen verbinden [3, 4]. Keine dieser Zellen zeigte aber eine spezifische Präferenz für eine bestimmte Bewegungsrichtung. T4- und T5-Zellen sind also die ersten Zellen in der Verarbeitungsbahn, welche richtungsselektive Antworten zeigen. Sie sollten somit dem Ausgang des Multiplikators des Modells entsprechen. Der entscheidende Schritt muss daher in der Verbindung zwischen diesen Zellen und den T4- bzw. T5-Zellen passieren. Momentan laufende Untersuchungen beschäftigen sich mit der Frage, welche dieser Zellen dem verzögerten und welche dem nicht-verzögerten Arm des Hassenstein-Reichardt-Detektors entsprechen. Die nächste, ebenso wichtige Frage ist die nach dem biophysikalischen Mechanismus, der diese Signale miteinander multipliziert. Hier werden zur Zeit zwei Möglichkeiten diskutiert: Zum einen könnten die Signale sich multiplikativ verstärken, wenn die Bewegung entlang der Vorzugsrichtung der Zelle läuft (‚Vorzugsrichtungs-Verstärkung‘). Zum anderen könnten sich die Signale spezifisch auslöschen, wenn die Bewegung in die Gegenrichtung läuft (‚Nullrichtungs-Unterdrückung‘). Beide Mechanismen könnten formal wie eine Multiplikation der Signale aussehen.
Die Antworten auf diese Fragen werden in naher Zukunft dazu führen, dass wir an einem einfachen Beispiel verstehen, wie das Nervensystem auf der Ebene einzelner Nervenzellen und ihren präzisen Verknüpfungen eine neuronale Berechnung durchführt, die für das Überleben des Individuums von entscheidender Bedeutung ist.



